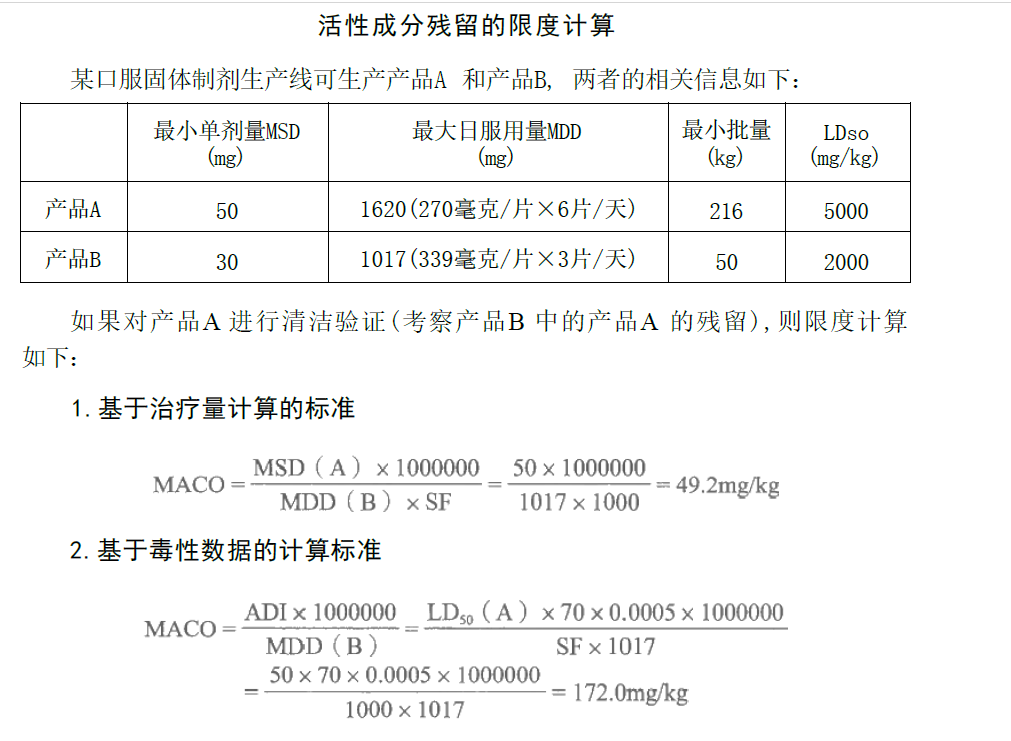
各位老师,这个MDD,嘿,好多老师的理解不一样,有的老师理解的是制剂的重量,有的老师理解的是下一活性成分的量。各位元老师,你们怎么看?
要讲逻辑原理噢,不能说什么指南说了,相关指南我已经看过了,要讲逻辑性与科学性。
懂的老师回答,不要讲什么按制剂的量这样算最严格,按最严格的来就行,这么讲就没意思了,拾人牙慧,因为我比如做成多个剂型的或同一剂型活性成分一样,但制剂量差别很大,比如:一个活性成分,就算是同一剂型,我一个做成50mg(活性成分含1mg),我一个做成500mg(含活性成分1mg)这能一样??
要讲科学推导。
懂的老师回答,不要讲什么按制剂的量这样算最严格,按最严格的来就行,这么讲就没意思了,拾人牙慧,因为我比如做成多个剂型的或同一剂型活性成分一样,但制剂量差别很大,比如:一个活性成分,就算是同一剂型,我一个做成50mg(活性成分含1mg),我一个做成500mg(含活性成分1mg)这能一样??
老师,我提一下我的一些个人理解,如有不对的地方,请指正。
1、清洁限度的制定核心原理就是找到一个可接受的安全总量,也就是所谓的MACO值。如果以上一产品为A,下一产品为B,那么关注的就是A在B中的最大允许安全的残留总量。假设A,B产品都在同一条生产线进行生产。且A的毒性明确,那么我们控制的目标就是A在B中的残留值,不能超过A的毒性标准。所以当A生产清洁结束后,这条生产线中残留的A的量是一定的。那么如何评价A的残留是否会对B造成影响呢?这时候就和B产品的批量和服用剂量相关了。首先说如果B产品的批量越大,就说明一定量的A在B中占比会越低。这时候当患者服用B的时候,间接进入患者体内的A就越小,此时就约安全。所以反过来说,当我们既定A的毒性了,我们就可以知道设备上残留A的最大允许残留比例,进而制定A在B中的最大允许安全的残留总量。
2、如果这个逻辑关系说清楚了,我们再关注公式中的另一个参数,就是服用剂量。这时候如果B产品的服用剂量越大,就说明一定量的A在B中占比会越低。也就是说患者在服用大剂量B产品的时候,间接进入患者体内的A就越多,此时就约不安全。所以反过来说,当我们既定A的独行了,我们就可以知道设备商残留A的最大允许残留比例,这时候的逻辑是B的口服剂量越大,对应的A在B中的最大允许安全的残留总量就约低。
3、在明确了1、2条中阐述的MACO值与批量、剂量的关系后,我们就正式探讨老师的问题。以老师的举例来看,当A产品毒性明确的前提下,后续产品如果把50mg(活性成分1mg)作为B产品,把500mg(含活性成分1mg)作为C产品,那么针对B,C两种场景的话,在制定清洁最大可允许残留时,这时候应该代入最大服用剂量,因此明显C产品的要求会更加严格一些。反过来说,如果按照老师的理解,都是用B,C的活性1mg的情况下,对应的清洁标准结果就是一致的了。一致的后果就是,明显患者在服用C产品的时候摄入了更大量的A,因此会对患者安全造成影响的。
从健康角度是这样的吧,他与人的摄入量有关呀?就像你说的如果是均匀分布,残留量是没有变的,但残留浓度是和制剂的日摄入量有关的,这样人的日摄入量才会一致?
因为 不管是千分之一 10ppm 还是PDE 都是评估的日摄入量。
另一个就是你说的限度 需不需要这么低? 个人觉得的确不需要任何品种都拿这个公司来算最低的,所以现在有了PDE的加入。 反过来想 从法规角度 他也不敢放得太宽,所以就有了现在这些同一的标准,这样管理和执行都 比较方便。
现在企业 是算的所有品种中最大的残留量,如下一产品MDD是最大的,下一产品批量是最小的。这个是很严格了。 我一直在想是不是可以用各自的MDD浓度来X各自的最小批量,,最后来选一个最大允许残留量就行。但未敢尝试。
按照APIC 清洁验证指南 或者 GMP附录 口服固体制剂 清洁验证章节,MACO公式都是:

其中:
MACO代表产品A能进入到产品B中的最大可接受量(mg);
MBS代表B产品的最小批量(ml或g);
TDDprevious代表A产品的日最小治疗剂量(mg)以API含量表示,等于每日服用产品A的最小数×规格
TDDnext代表在设备中生产B产品的最大日剂量(ml或g)以制剂的量标识,等于每日使用产品 B 的最大数×单个制剂的质量或体积
SF代表安全系数,可取1000。
个人理解:
最小批量÷B产品最大剂量=使用到下一产品(B)最少患者数量
当认为产品b中残留的a,其限度为a最小日剂量1/1000是是安全的(sf:1000),那么产品a在产品b下一批次(最小批次)中残留限度的MACO计算就是:b可能用到的患者数量乘以每个患者用产品a残留的安全剂量
最少患者数量×上一产品(A)日最低剂量/10000可得到产品A残留总量
按照以上逻辑,产品A 最大剂量 (按规格表示): 产品B最大剂量(按规格表示),这个比值本身没有意义,需要加入产品b的批量。故题主计算是 产品b用api 规格或者 制剂总量均可,在计算产品b 批量时统一即可,如都按api量:api规格 或者 制剂配制总量:制剂总量,最终结果是一致的。
上面可能表述不太清楚
当认为产品b中残留的a,其限度为a最小日剂量1/1000是是安全的(sf:1000),那么产品a在产品b下一批次(最小批次)中残留限度的MACO计算就是:b可能用到的患者数量乘以每个患者用产品a残留的安全剂量
最少患者数量×上一产品(A)日最低剂量/10000可得到产品A残留总量
按照以上逻辑,产品A 最大剂量 (按规格表示): 产品B最大剂量(按规格表示),这个比值本身没有意义,需要加入产品b的批量。故题主计算是 产品b用api 规格或者 制剂总量均可,在计算产品b 批量时统一即可,如都按api量:api规格 或者 制剂配制总量:制剂总量,最终结果是一致的。
这{{threadTextType}}正{{isAdminText}}
为帮助审核人员更快处理,请填写举报原因:
为帮助审核人员更快处理,请填写举报原因: