3个回答
法规现在基本没有规定再验证周期,提的概念是定期评估。
例如:中国GMP附录《确认与验证》要求:“对设施、设备和工艺,包括清洁方法应当进行定期评估,以确认它们持续保持验证状态”。
摘录如下:
Q1. 如何开展设备、设施的定期审核评估?
— 关于非法规/指南等强制的再验证周期设备设施,如何开展定期审核评估和周期的确定?
向导@圣人有点冷:
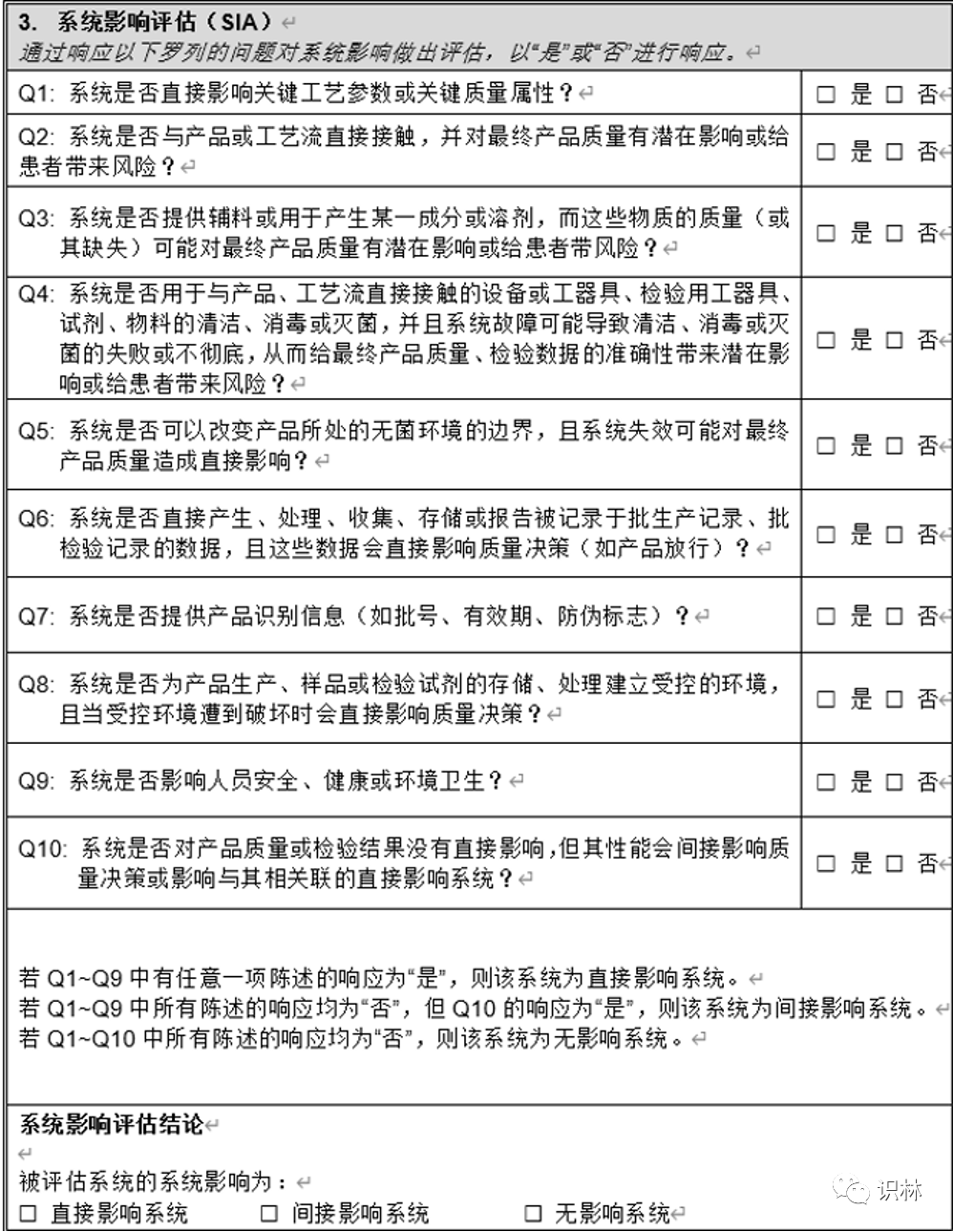
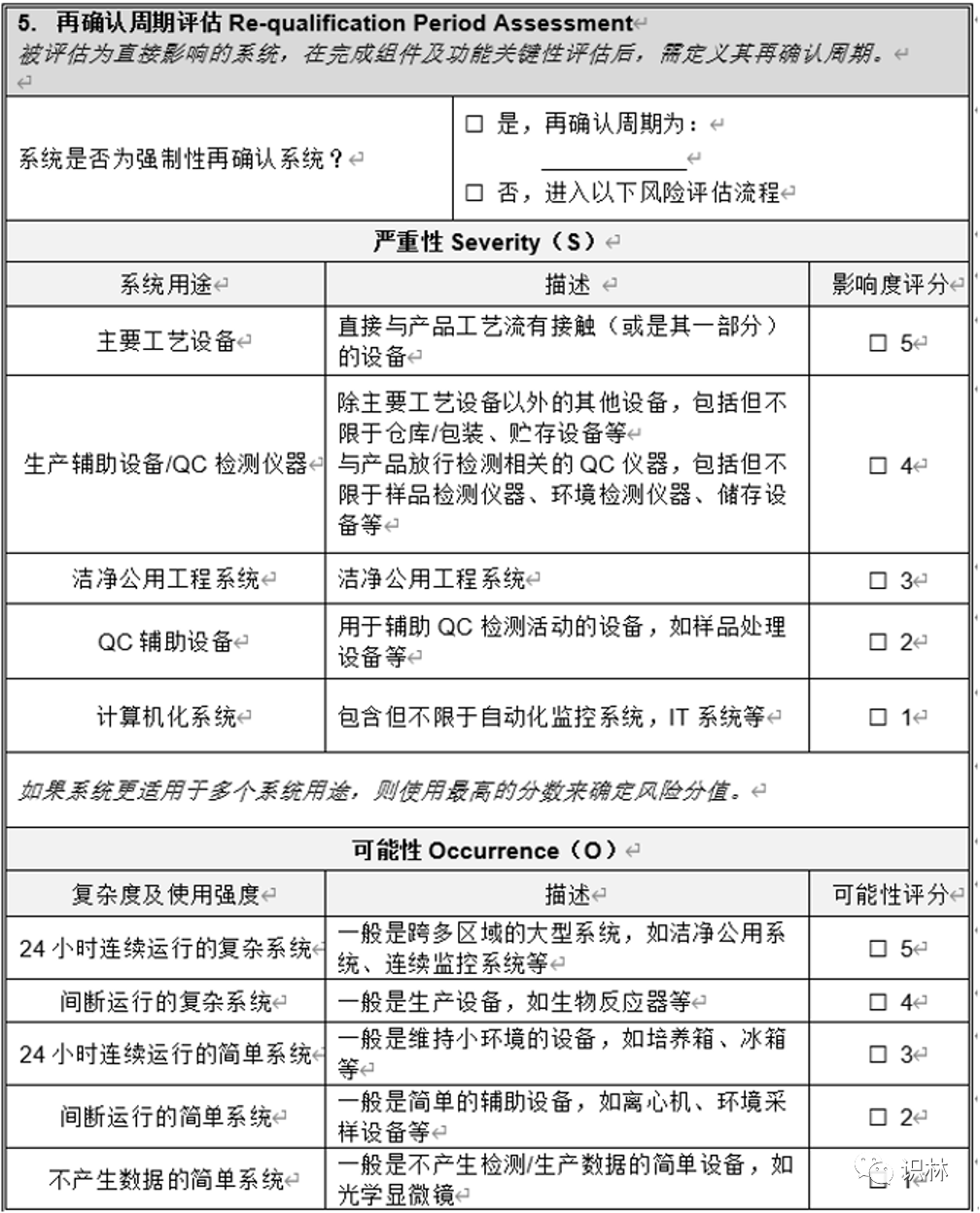
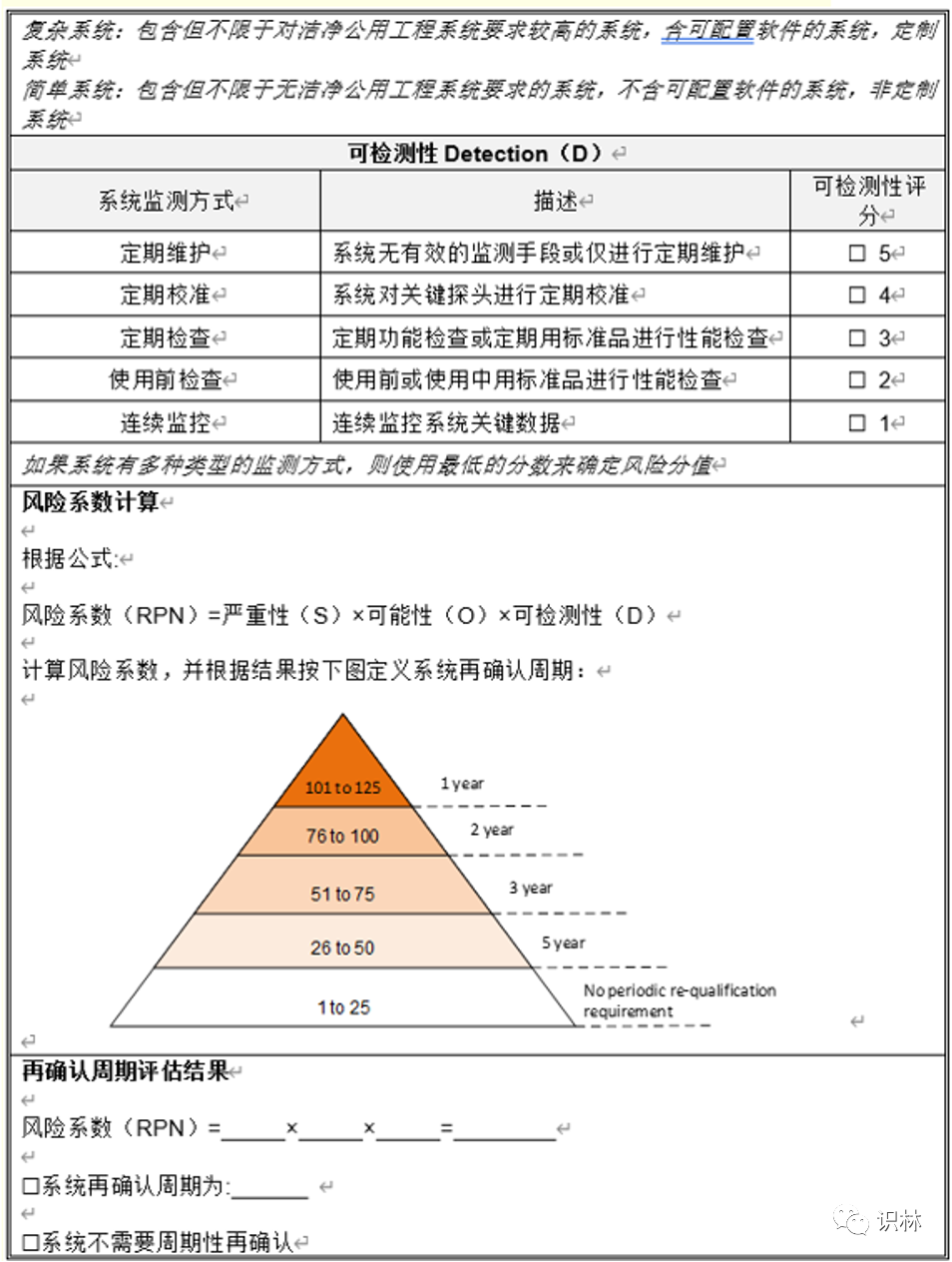
需对设备的关键性进行评估,可参考ISPE调试与确认(第二版)系统影响评估(8个问题),对系统进行分级,分为之间影响系统、间接影响系统、无影响系统,评估为直接影响系统的再对其进行再确认周期的判定,分为强制再确认周期,这个是法规规定的,如灭菌器,A级洁净区空调等;非强制性,根据系统的风险,从严重性、可能性、可探测性进行打分并计算RPN。根据RPN确认再确认周期。
同一台设备根据其使用的用途可以制定不同确认周期,例如冰箱,在仓库、生产和QC实验室储存的物料是不一样的,自然风险也不一样。
评估可参考下表:
评论
匿名
提交
取消
匿名
{{item_parent.created_at}}
置顶
批准
驳回
编辑
等待审核
已驳回
回复
{{item_parent.show_reply_list ? '收起回复' : '查看回复'}}({{item_parent.children.length}})
编辑
提交
取消
写回复
匿名
提交
取消
{{item_children.from_user}} 回复 {{item_children.to_user}}
{{item_children.created_at}}
批准
驳回
编辑
等待审核
已驳回
回复
编辑
提交
取消
写回复
匿名
提交
取消
这{{threadTextType}}正{{isAdminText}}
举报
提交
取消
为帮助审核人员更快处理,请填写举报原因:
举报
提交
取消
为帮助审核人员更快处理,请填写举报原因: