7月23日CDE发布的风险分析与管理计划撰写指导原则(征求意见稿),正文中有一行需要填写该药物的全球首次获批时间,请问大家是如何快速准确的查询到这个结果?
1. 收费数据库:
如果贵公司购买了例如Cortellis、Pharmaprojects等收费数据库,那么查询绝大多数药物的全球上市时间就比较容易了,在数据库中直接检索即可,不再赘述。
2.免费检索途径:
免费检索途径相比收费数据库会更费时且需要一些技巧,有时可能需要同时结合多种途径相互佐证,主要的途径有如下几种:
(1) 搜索引擎:
此方法是最直接的方式,推荐使用Google或Bing等搜索引擎,以英文关键词“药物名称+first launched/approved/marketed/developed/introduced”检索,通过搜索出的文章或者文献来获取某药物的最早上市时间。
以依达拉奉为例,在Google中搜索“edaravone first
launched”,可以搜索出多篇官方或非官方的文章或文档,都可以确定该药物最早于2001年在日本上市。
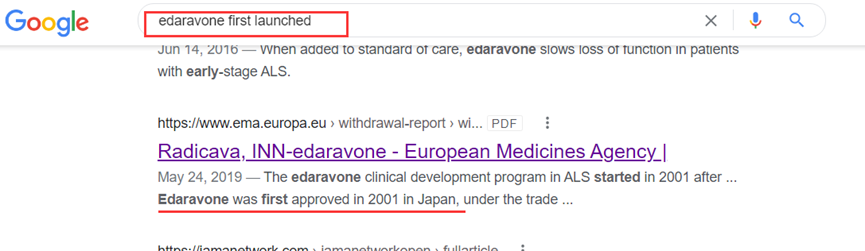
此方法适合大多数药物的检索,但是信息的准确度需要根据信息来源是否可靠进行评估或通过下述其它检索方式进一步确认。
(2) 上市公司年报查询
由于上市公司需要向投资者披露公司的信息,因此可以在上市公司年报中查找某药物的批准情况。此方法适用于查询近年来上市公司的一些新药,上市时间比较久远的药物一般不适用。在确定某药物的原研公司后,查询该公司是在哪个国家或地区的证券交易所上市,可选择在监管机构或上市公司官网下载该公司年报文件。
这里只举例比较常见的在美国证券市场上市的情况,以Intercept制药公司的OCALIVA为例:
SEC网站下载:不管是在纽约证券交易所(NYSE)还是纳斯达克证券交易所(NASDAQ)上市的公司,都归美国证券交易委员会(SEC)监管,因此可在SEC官网下载年报文件,直接在SEC官网搜索公司名称或股票代码就可以搜索出公司相关披露文件,。需要注意的是,注册地在美国的公司年报为10-K文件,季报为10-Q文件,注册地在美国以外的公司年报为20-F文件,选择相应的文件下载即可。
官网下载:除了SEC以外,上市公司一般会在官网的Investor
Relations (IR)板块提供年报文件下载。进入Intercept公司官网,点击上方“INVESTORS & MEDIA”进入IR页面,

再点击左方的“FINANCIAL INFORMATION”

进入财务信息页面后即可下载年报10-K文件。

无论是通过SEC还是官网下载Intercept公司的2021年报文件后,可以在其中找到关于OCALIVA的上市情况,可以看到OCALIVA最早是在2016年5月在美国被批准上市,2016年12月被欧盟批准.从2017年1月开始,陆续获得加拿大、以色列和澳大利亚等国批准。

有些时候在最新的年报文件中无法找到某药物的最早上市信息时,可以多往前翻几年的年报也许可以找到相关信息。因为是原研公司自己公布的信息,所以本检索途径相对于其它途径来说是最准确的,但有些药物的最早上市时间可能通过此途径无法获得
(3)日本IF文件
上市相对久远的药物的相关信息总是很难检索,这时我们可以借助日本的IF文件来获得信息。药品研发人员多通过检索日本IF文件来获得在日本上市药品的处方、包材、稳定性等药学信息(IF文件具体下载方法请参考网上相关教程,不再赘述),但其实日本IF文件是由固定格式要求的,其中 “開発の経緯”部分可以看到该公司对某药物上市历史情况的综述,而“主な外国での発売状況”部分中则是该药物在日本国外的上市情况,如果是原研的IF文件,那这两个部分内容均较为准确。如果是仿制药的IF文件,则本部分内容可作为参考。
例如,注射用阿奇霉素。化合物最早是由PLIVA公司开发并授权给辉瑞公司进行部分地区的销售,该药物上市时间较早且有多种剂型和规格。打开辉瑞公司注射产品的IF文件,可以看到在“開発の経緯”部分中详述了此药物的开发过程,可以看到辉瑞公司的注射剂最早是于1997年在美国上市。

而在“主な外国での発売状況”我们可以看到各主要国家的上市时间,同样也可以确定最早上市时间。
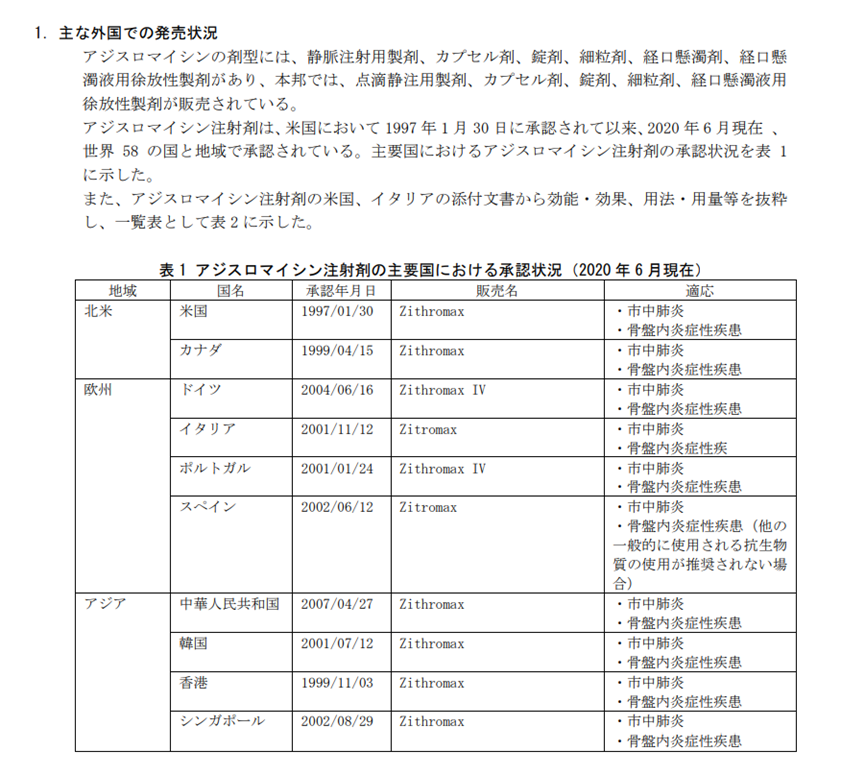
该方法只适用于在日本由上市的药物,尤其是日本公司参与研发的药物“開発の経緯”部分会撰写的非常详细。但有时原研公司可能只会写出在日本的开发背景,不会写出全球的上市情况,这时需要结合其它方法来进一步确定。
(4) 免费数据库
有一些免费数据库也可以检索药物的上市情况,例如Drugbank等数据库,可参见此页其它回答中的检索方式。但是免费数据库中的数据可能存在不准确或不全面等问题,所以需要同时结合其它方式确定。
(5) 各国药监局查询
此方法是通过对全世界主要国家或地区(中国、美国、欧盟、日本、韩国、俄罗斯、加拿大、阿根廷、巴西、瑞士等)的药品监管部门进行穷举式的检索来确定,此方法较为费时,各国家上市药物查询方式请参考网上相关教程,此处不再赘述。
但是,此方法可以作为以上任一方法的补充或者作进一步确认时使用。
我们公司会订购专业数据库,比如Cortellis,科睿唯安下面的竞争情报数据库。以利伐沙班(Rivaroxaban)为例,进去后,就会显示历史获批信息。可以看到,最早是2008年在加拿大获批。所以看公司是有有经费用于数据库的采购。
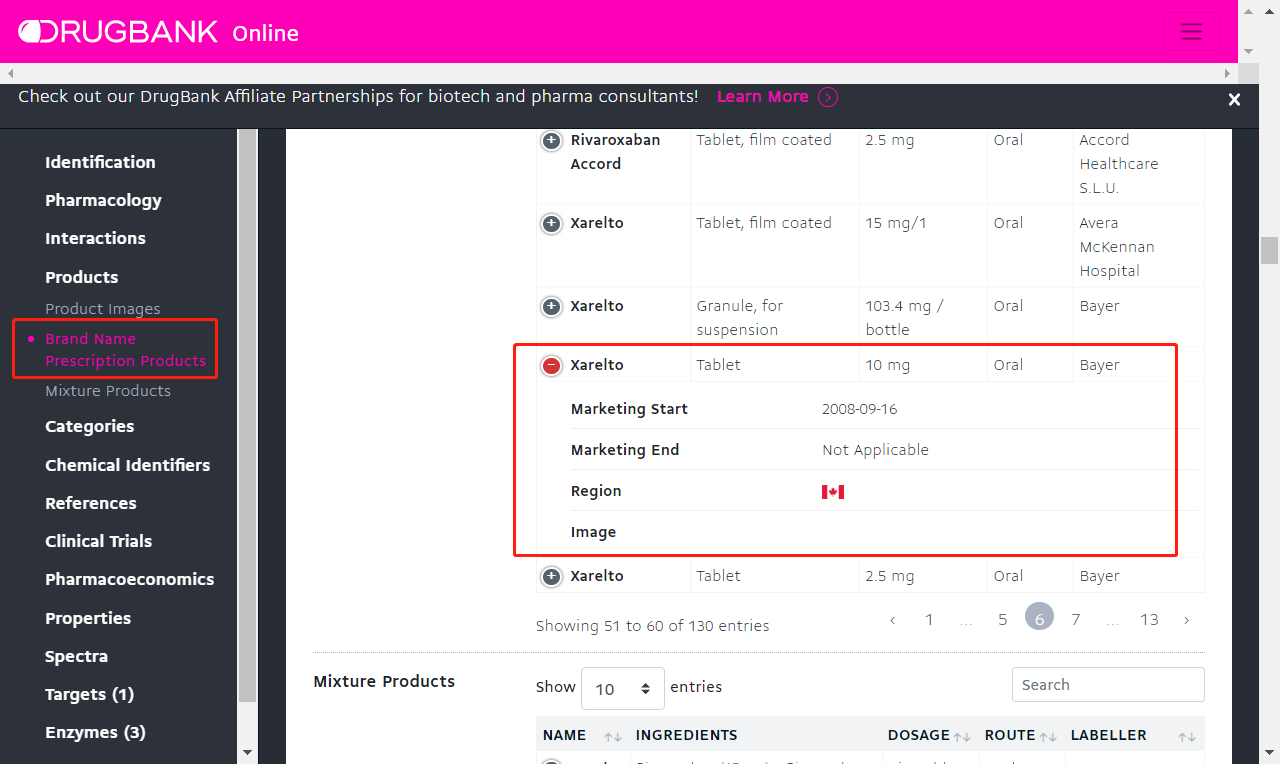
如果要免费的话,推荐一个网站,Drugbank。https://go.drugbank.com/ 输入产品名称后,会出现搜索结果。在左边导航栏选择 Product → Brand Name Prescription Products,会出现所有上市的产品信息。对于这种大品种,有很多生产企业(Drugbank里列了131条记录),就需要做些筛选。在原研公司项下,逐一打开每个记录前面的“+”,看获批时间。非常繁琐和费时,但是没办法,免费的话,我了解到的这个网站比较全,欢迎大家补充其他便捷的方法。对于只有原研品种,或者近几年批准没有太多记录的产品,这种方法还算方便。此外,该网站还能查询产品的理化性质、临床情况、靶点适应症信息等,非常全。
这{{threadTextType}}正{{isAdminText}}
为帮助审核人员更快处理,请填写举报原因:
为帮助审核人员更快处理,请填写举报原因:
