5个回答
选择密封性试验方法时,首先考虑包装内容物的特性,此外包装的设计结构、包装系统的材料、包装系统的密封类型以及最大允许泄漏限度等均会对方法的选择产生不同的影响。可结合药典委关于征求无菌药品包装系统密封性指导原则标准草案意见的函、已上市化学变更指原则,变更前后的研究结果综合评判。
这里给出一个海南省局关于检漏方式变更的问题,可供参考。变更化学制剂生产过程中包装密封性的检测方法,如色水法变更为真空衰减法,是否可以按照微小变更进行年报管理?

评论
匿名
提交
取消
匿名
{{item_parent.created_at}}
置顶
批准
驳回
编辑
等待审核
已驳回
回复
{{item_parent.show_reply_list ? '收起回复' : '查看回复'}}({{item_parent.children.length}})
编辑
提交
取消
写回复
匿名
提交
取消
{{item_children.from_user}} 回复 {{item_children.to_user}}
{{item_children.created_at}}
批准
驳回
编辑
等待审核
已驳回
回复
编辑
提交
取消
写回复
匿名
提交
取消
这{{threadTextType}}正{{isAdminText}}
举报
提交
取消
为帮助审核人员更快处理,请填写举报原因:
举报
提交
取消
为帮助审核人员更快处理,请填写举报原因:

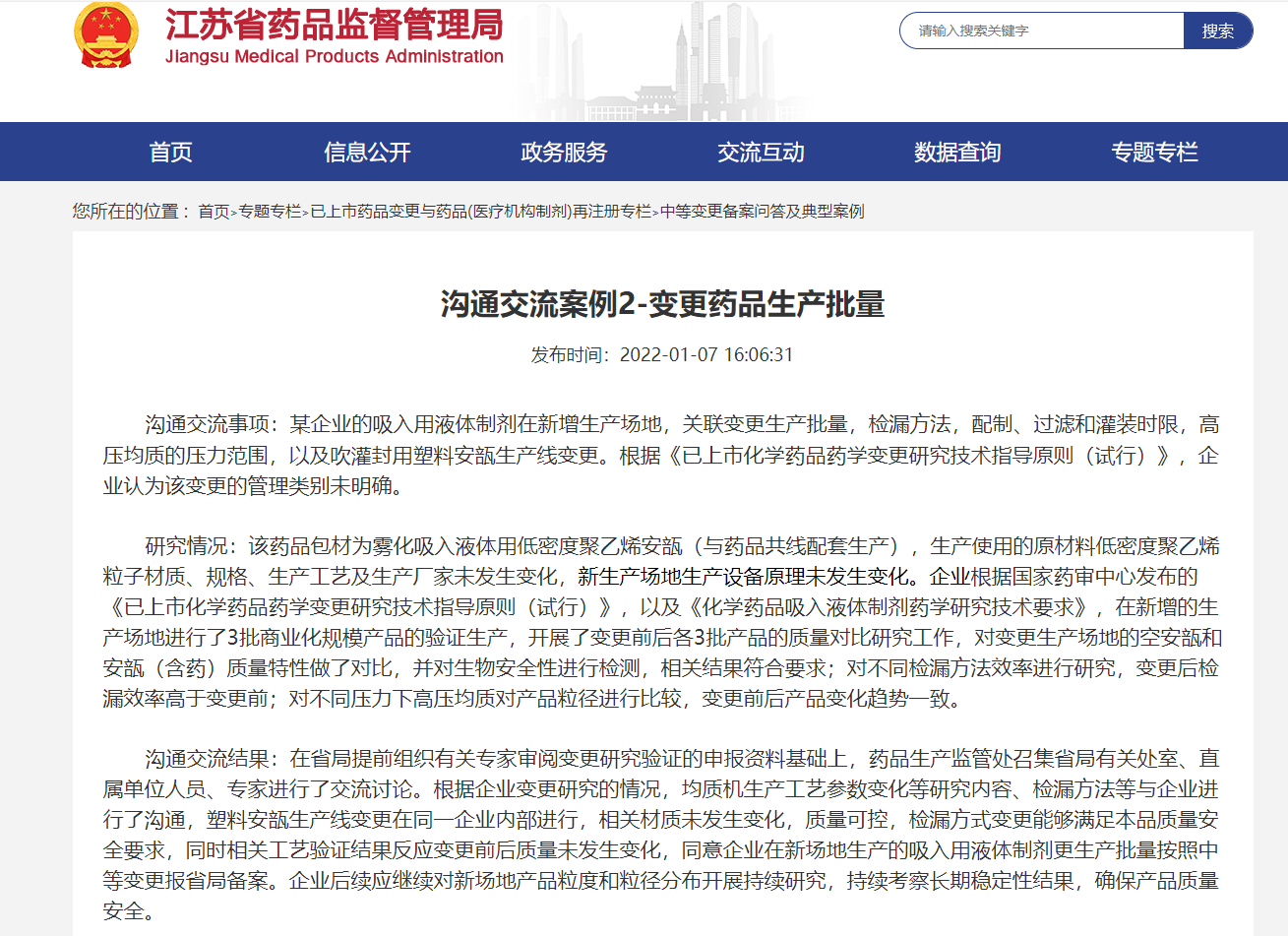 可以参考江苏药监局沟通交流案例
可以参考江苏药监局沟通交流案例