早期临床阶段与临床I期,临床II期的关系
QAQC临床研究
1.《药品生产质量管理规范》临床试验用药品附录中对早期临床定义为:是指临床药理和探索性临床试验,原则上应包括初步的安全性评价、药代动力学研究、初步的药效学研究和剂量探索研究。临床试验用药品制备所用原辅料及包装材料应当进行相应的检验或检查,合格后方可放行使用。对于早期临床试验用药品所用辅料及包装材料可凭供应商的分析报告接收,但至少应当进行鉴别。
2.总局关于发布药物临床试验的一般考虑指导原则的通告(2017年第11号)中有对临床药理、探索性临床、确证性临床试验、上市后研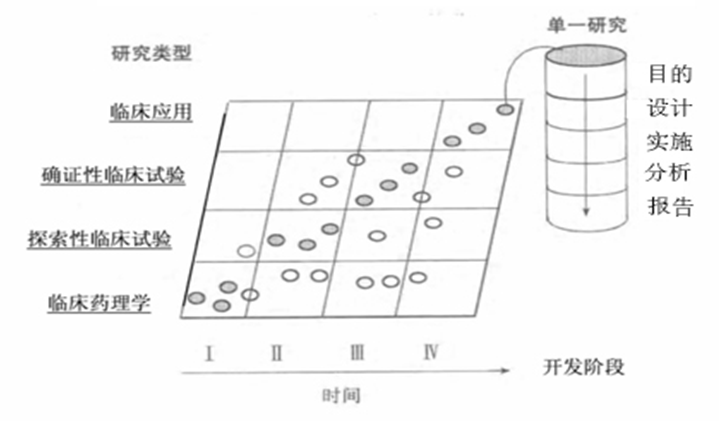 究与临床I/II/III/IV阶段对比关系,如图所示,实心圆代表在某一研发阶段最常进行的研究类型,空心圆代表某些可能但较少进行的研究类型。
究与临床I/II/III/IV阶段对比关系,如图所示,实心圆代表在某一研发阶段最常进行的研究类型,空心圆代表某些可能但较少进行的研究类型。
 究与临床I/II/III/IV阶段对比关系,如图所示,实心圆代表在某一研发阶段最常进行的研究类型,空心圆代表某些可能但较少进行的研究类型。
究与临床I/II/III/IV阶段对比关系,如图所示,实心圆代表在某一研发阶段最常进行的研究类型,空心圆代表某些可能但较少进行的研究类型。问题:是否可以根据实心圆确定早期临床就是指临床I期、临床II期研究?临床I/II期实验用药品所用辅料及包装材料科凭供应商的分析报告接受,但至少进行鉴别实验?
评论
匿名
提交
取消
匿名
{{item_parent.created_at}}
置顶
批准
驳回
编辑
等待审核
已驳回
回复
{{item_parent.show_reply_list ? '收起回复' : '查看回复'}}({{item_parent.children.length}})
编辑
提交
取消
写回复
匿名
提交
取消
{{item_children.from_user}} 回复 {{item_children.to_user}}
{{item_children.created_at}}
批准
驳回
编辑
等待审核
已驳回
回复
编辑
提交
取消
写回复
匿名
提交
取消
这{{threadTextType}}正{{isAdminText}}
举报
提交
取消
为帮助审核人员更快处理,请填写举报原因:
举报
提交
取消
为帮助审核人员更快处理,请填写举报原因:
