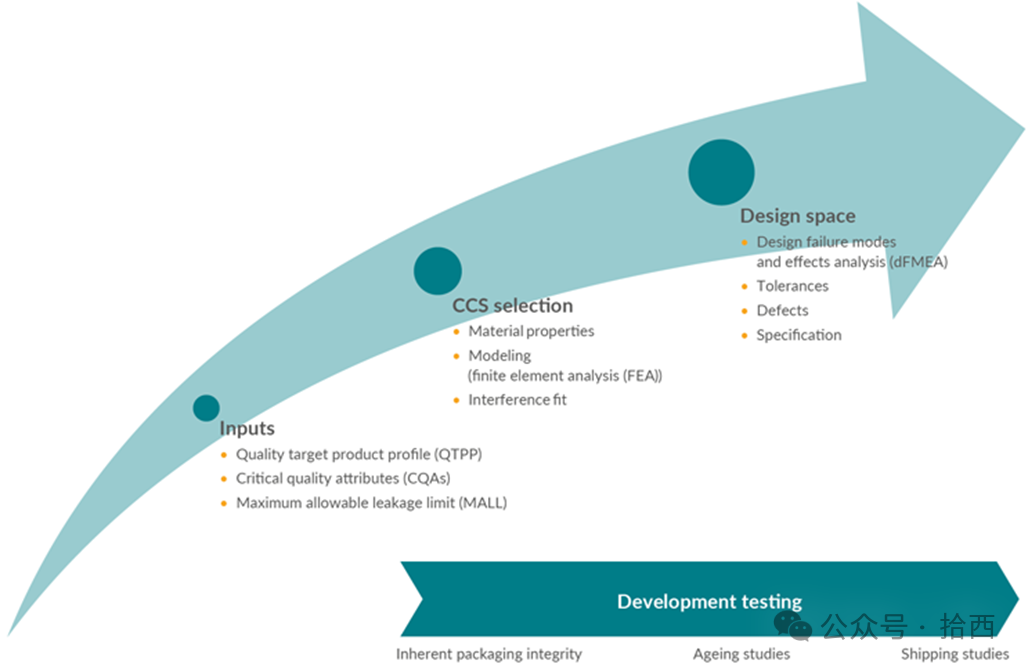
容器封闭完整性 (Container closure integrity,CCI) 是指容器封闭系统 (container closure system,CCS) 保持无菌屏障以抵御潜在污染物, 同时也防止从CCS向外泄漏的能力。可能穿过容器封闭屏障的污染物包括微生物和活性气体。CCS 必须在整个保质期内保持无菌药品、生物制品和疫苗产品的无菌性和产品质量。传统对其的期望是通过测试来证明控制,但当前的法规正在推动一种基于科学和风险的方法,这意味着将质量融入设计和流程中,而不是仅依靠测试/检查制造的产品。本文概述了建立综合性方法以确保 CCI 的最佳实践。对于新项目,这种优先关注点始于开发,并贯穿验证和制造。对于现有/已批准的项目,综合性方法将较少关注开发和验证,而是专注于制造,同时利用知识和经验来验证相关风险评估中详述的持续控制记录。它表明,对于CCI的综合方法可以为最终测试提供可行的替代方案。下根据产品生命周期的不同阶段进行介绍。在开发过程中,应选用选择适合药品的 CCS。开发团队确定 CCS 组件如何共同实现 CCI,以及组件的哪些方面有助于药品制造、运输和储存的密封性。这分三个连续阶段实现(见图 1),并得到开发数据的支持。
质量目标产品属性 (Quality Target Product Profile,QTPP) 和 CCS 选择
定义 QTPP 通常是药物产品开发的第一步。考虑选择合适的 CCS 和定义在哪些条件下需要确保 CCI 的关键输入。以下方面直接影响 CCI:
-
-
高压high-stress制造工艺(例如终端灭菌),
-
-
其他方面间接影响整体 CCI 方法的开发。例如,如果需要阻隔涂层来减少可浸出物,开发团队需要评估橡胶密封件和容器之间减少接触的影响。
最大允许泄漏限值 (Maximum Allowable Leakage Limit,MALL)
MALL 是给定产品包装可容忍的最大泄漏率,不会对产品安全造成风险,也不会对产品质量造成影响(或影响不大)。具体而言,CCI 损失可能会产生以下影响:
-
-
产品剂量溢出或外部液体或固体物质进入,导致产品理化质量属性失效,
-
气体顶部空间含量的变化,导致产品理化质量属性的失败,以及
-
需要考虑产品的 QTPP,正式评估CCI 损失的严重程度。初始 CCS 特性分析的重点是确定可能影响系统在不同条件下稳定性的技术方面。通常,这是通过纸面分析、计算机模型和探索性测试来实现的。探索性测试的样本量由工程师自行决定,并应在此阶段根据需要进行调整。此阶段的目标是了解组件如何密封容器,特别是通过识别密封表面。一旦通过初始 CCS 特性确定了缺陷和尺寸要求,就应与潜在供应商一起审查缺陷和尺寸要求,以确保他们能够满足规定的要求。这些组件要求和其他期望应记录在组件规范或供应商质量协议中。风险评估是 CCS 开发的一部分。此操作不仅限于 CCI,还将 CCI 相关风险与QTPP 得出的其他基本要求相结合。关于 CCI,风险评估结合了从初始特性描述中学习到的知识和 QTPP 中提到的条件。风险评估可以考虑以下方面:为确保开发方案的全面性,所有已识别的风险都应通过特性研究来支持,以更好地了解流程并制定适当的控制策略。扩展的特性数据直接支持风险评估评级。需要合理的实验设计和适当的样本量。只要药品不影响容器的完整性和/或功能性,就可以考虑采用空或充满水的 CCS 平台方法进行所有开发测试。众所周知,高 pH 值、保存的配方或冷冻产品可能会产生额外的风险。此种产品可能会在项目生命周期的后期考虑,这可能会影响方法的选择。
组合产品Combination Products设计验证
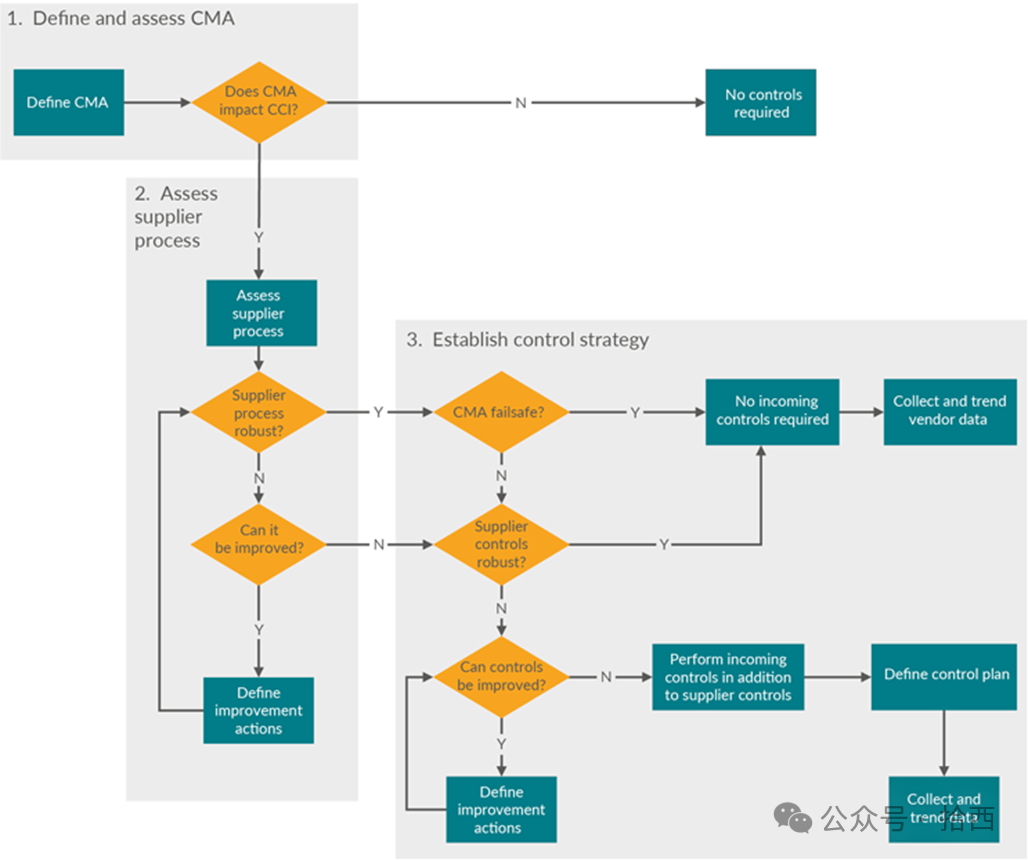
对于用于组合产品的 CCS,扩展特性分析工作将作为设计验证活动的一部分进行。只要有可能,根据质量源于设计而开展的开发活动就应考虑利用整体控制策略。如果所谓质量源于设计的活动没有考虑到设计控制过程的需求时,就会变得很有挑战性了。考虑组件制造和加工对整体 CCI 的影响。图 2 是一棵决策树,有助于定义关键材料属性 (critical material attributes,CMA) 和供应商控制策略。风险评估的输出确定了需要维护和控制的 CMA。这些可用于评估供应商流程如何影响 CMA。与所有制造流程一样,初级包装组件的生产也存在变化,可能会导致组件不适合使用。因此,了解初级包装组件供应商流程及其操作范围至关重要,以确保在组件制造和供应商放行期间实施适当的预防和控制。
评估供应商工艺——组件制造过程中供应商的预防和控制
CMA 允许在评估供应商制造工艺是否存在潜在危害时制定控制策略。这是为了在供应商放行和生物制药制造商随后验收时保持适当的组件质量。如果 CMA 在设计上不符合规范的可能性较低,则可将其视为一种安全措施。基于对主要包装组件供应商制造过程的全面分析,可以制定和实施全面组件控制策略。这可以基于确认供应商质量体系充分,并采取预防和控制措施和/或生物制药制造商组件发布规范中要求的额外测试。对供应商过程故障模式和影响分析(pFMEA) 文件的审查应深入了解现有控制计划的基础以及计划持续改进的程度,以提高过程稳健性。根据相关法规指导,工艺验证 (PV) 在产品生命周期内分为三个阶段:工艺设计 (第 1 阶段)、工艺效果确认 (第 2 阶段) 和持续工艺验证 (第 3 阶段)。PV/工艺性能效果确认 (PPQ) 意味着收集和评估数据,以建立科学证据,证明工艺能够持续提供预定质量的产品。CCI 的综合性方法与上述做法一致。如果将其应用于 CCI,初始工艺设计(第 1 阶段)将涉及初始 CCS 开发和组件装配工艺的认证,包括可加工性或工程运行以定义制造工艺。了解 CCI 中的组件变异性和 CMA知识是 CCS 开发的关键输出,可用于定义规范并实施围绕主要容器输入的控制。这些是全面 CCI 验证策略的重要元素,应在进行 PV/PPQ 之前定义。组件确效的目的是评估组件制造过程中的常规验证对 CCI 的影响有多大。在 PV/PPQ 之前,应确定将单个包装组件转换为完全组装的 CCS 所涉及的关键工艺步骤。这些工艺步骤可以作为组件准备的一部分或在灌装/密封期间执行。确定工艺步骤后,建议在 PV/PPQ 之前对整个 CCS 组装工艺进行确效,以证明每个工艺步骤中涉及的工艺目标、设备设定点和操作范围可以可靠地生产出满足其关键质量属性的完整 CCS。我们建议这些确效研究涉及挑战参数操作范围的上限和下限,以评估对 CCI 的影响。
-
总体而言,PV/PPQ 的目标是确认控制策略的有效性,并且预期的 CCI 验证所输出的信息是科学证据,证明 CCS 在商业制造过程中组装时将满足关键质量属性。
-
与包装组件输入、设备和工艺参数相关的控制源自成功完成的效果确认活动,并且在进行PV/PPQ 之前就已经到位。
-
最终,PV/PPQ 应该通过所选的包装组件输入和商业制造过程证明 CCI,充分模拟工艺负载压力以确认控制策略的有效性/稳健性。
-
成功的无菌工艺模拟APS的结果可以作为CCI 性能的额外证明,而无需进行微生物侵入测试。
-
PPQ 批次通常用于确认先前研究中所开展的保质期评估。
制造过程对于创建和维护 CCI 至关重要。经过深思熟虑并实施的综合控制策略将消除制造过程可能对 CCI 产生不利影响的风险。从整体上看,良好的制造控制策略最常见的步骤是精心设计的预防措施。如果预防措施本身不能消除 CCI 的所有风险源,则应辅以良好的过程控制。任何制造后测试都只能作为制造过程受控的高阶确认,但制造后测试不能证明产品质量良好。在药品整体 CCI 方法下,影响CCI 的大多数因素都已纳入 CCS 的开发以及稳健的产品制造工艺中。这种方法的另一个要素是在整个产品保质期内直至使用时证明 CCI,以证明无菌产品没有微生物污染。一旦确定了最终的包装配置,运输/装运研究通常会在产品开发过程中作为提交的一部分一次性执行。以上内容概述了如何制定全面的整体战略以确保 CCS 的 CCI。这项工作不应被视为一次性活动;建立健全的监测和持续改进流程同样重要。建议的做法是确保将技术考虑因素纳入药品质量管理体系。对肠外药物产品采用综合性方法进行 CCI是与质量源于设计的原则完全一致。合适的 CCS 的关键功能之一是提供一个完整的容器,该容器将根据其 QTPP 在整个生命周期内保护药品,并防止从 CCS 泄漏。肠外产品 CCI 采取综合性方法描述了如何在产品生命周期内实施质量,而不是依赖于最终产品发布和稳定性测试。这种整合建立在正式的风险评估之上,涵盖药品的 CCS 设计和开发、验证、常规制造、稳定性和运输。
作者:Shengyi
来源:拾西
公众号日期:2024年6月5日