2023.09.12 最近因为工作的原因在学习日本的法规,扒了扒MHLW和PMDA日文版的网站,供参考。更多补充后续更新。
|
药监机构1 |
名称 |
厚生劳动省(MHLW,Minister of Health, Labour and
Welfare) |
|
官网 |
日文:https://www.mhlw.go.jp/index.html 英文:https://www.mhlw.go.jp/stf/english/index.html 日文网站信息较多 |
|
|
简介 |
厚生省最早设置于1938年,2001年与劳动省合并,并改为厚生劳动省,是负责日本医疗卫生和社会保障的主要部门。厚生劳动省设有11个局,主要负责日本的国民健康、医疗保险、医疗服务提供、药品和食品安全、社会保险和社会保障、劳动就业、弱势群体社会救助等职责。 |
|
|
药监机构2 |
名称 |
药品医疗器械局(PMDA,Pharmaceuticals and Medical Devices
Agency) |
|
官网 |
日文:https://www.pmda.go.jp/index.html 英文:https://www.pmda.go.jp/english/index.html 日文网站信息较多 |
|
|
简介 |
2004年4月1日,正式成立了药品医疗器械局,其职能主要有以下三项:一是药物不良反应救济职能;二是审查医药品与医疗器械的相关职能,包括对新药械的报批进行审查;对临床试验提供指导与建议;审查进行GLP与GCP所必需的申请书;对生产设备、流程和质量控制进行GMP检查;三是确保药品安全职能,包括收集、分析、公布关于药械的质量、有效性和安全性的信息等。 |
|
|
监管范围 |
医疗用医药品(处方药)、一般用医药品/要指导医药品(非处方药)、医疗器械、再生医疗等产品、体外诊断用医药品、医药部外品、化妆品 |
1.
医薬品医療機器法
日文版:厚生劳动省的法令数据库(https://www.mhlw.go.jp/hourei/index.html)按目次搜索
 |
→ |
 |
英文版:日本法律翻译(https://www.japaneselawtranslation.go.jp/en)可以搜索关键词pharmaceutical

搜索结果绿色框出的内容,可以大致窥见日本的法律体系:
- 最高层级是国会发布的“药品医疗器械法”法律
- 第二层级是内阁发布的“药品医疗器械法施行令”政令
- 第三层级是MHLW发布的“药品医疗器械法施行规则”省令 —— GMP也属于这一层级
- 再往下级还有通知等(比如PMDA发布的通知,可在PMDA网站查看)


2.
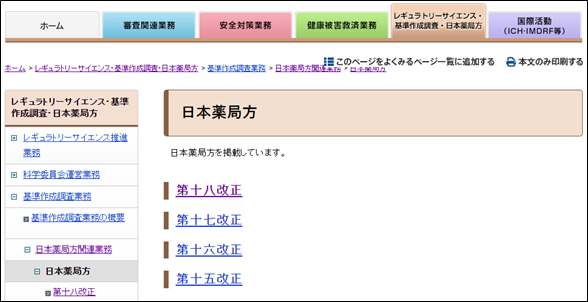
薬局方
日本药典(JP),目前是第十八版,日文和英文版都可以在PMDA网站下载(https://www.pmda.go.jp/rs-std-jp/standards-development/jp/0004.html)
3.
PMDA网站审查相关业务介绍(https://www.pmda.go.jp/review-services/outline/0001.html)

- PMDA网站各项目,有介绍、流程、所需资料、模板、费用等信息
- 国外所有的申请都需日本国内管理人(In-country caretaker, ICC)
3.1
外国制造商认证(Accreditation of foreign
manufacturers, AFM)
国外生产厂商进行申请前必须先完成国外制造厂商认定程序(Accreditation of foreign
manufacturers,AFM),获得认定证书。
- 分类、流程、资料、费用https://www.pmda.go.jp/review-services/drug-reviews/foreign-mfr/0009.html#procedure
- 需要检查(书面或现场)、每五年更新一次、有变更时也需要申请。
- 通过认证的制造商查询:https://www.pmda.go.jp/review-services/drug-reviews/foreign-mfr/0003.html
3.2
MF登记制度
MF 登记程序不仅适用于药用原料药,还适用于中间体、药用辅料、医疗器械原材料和药包材等(OTC药品使用的原料药、中间体和辅料不适用,OTC使用新原料药除外)。
- 流程、资料(模块三,分公开和保密部分)、无需费用https://www.pmda.go.jp/review-services/drug-reviews/master-files/0002.html
- 时限:受理后约15天(不保证15天以内)获得登记证。申请制剂需要原辅料的MF登记号时,请在制剂的申请日之前预留约1个月的富裕时间进行MF登记。
- 已登记MF查询:https://www.pmda.go.jp/review-services/drug-reviews/master-files/0008.html
4.
GLP/GCP/GMP等
这些均属于省令,英文版可获得(https://www.pmda.go.jp/english/review-services/regulatory-info/0001.html):

如果想找日文版,简单的方法是根据英文版的发布时间,在日文的法规检索中找相应日期的日文法规,例:


5.
已获批产品查询
日文版PMDA网站上方,可检索,但必须是日文名:

英文版PMDA网站的“List of Approved Products”仅可按年份查找

为帮助审核人员更快处理,请填写举报原因:
为帮助审核人员更快处理,请填写举报原因:

补充一下,PMDA上查询必须使用日文名,一般我使用药智数据库查询
JP的对照品在哪里查询效期或者是否换批?