举报
提交
取消
为帮助审核人员更快处理,请填写举报原因:
评论
匿名
提交
取消
匿名
{{item_parent.created_at}}
置顶
批准
驳回
编辑
等待审核
已驳回
回复
{{item_parent.show_reply_list ? '收起回复' : '查看回复'}}({{item_parent.children.length}})
编辑
提交
取消
写回复
匿名
提交
取消
{{item_children.from_user}} 回复 {{item_children.to_user}}
{{item_children.created_at}}
批准
驳回
编辑
等待审核
已驳回
回复
编辑
提交
取消
写回复
匿名
提交
取消
举报
提交
取消
为帮助审核人员更快处理,请填写举报原因:

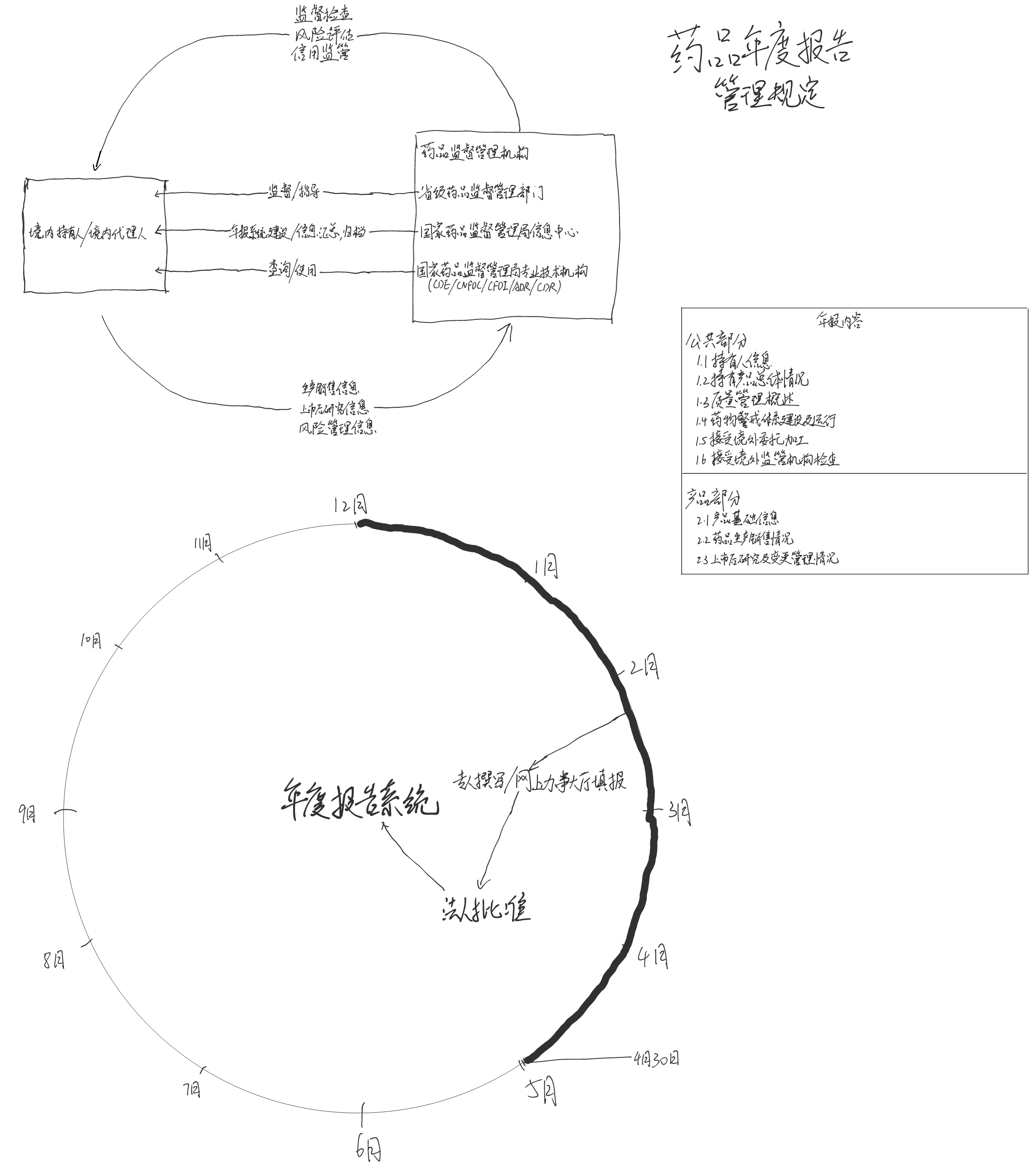
很赞,如果能基于企业实践,把最详细最实际的SOP转化为这种形象化的流程图,可上主站了。
年报将是长期热点,给所有RA增加了一项固定工作。
报告提交日期有原来的3月份延长到4月份了
好文章。。。。。。。。。昊河哈文医 管
想请问,“上市后研究”包括哪些监管要求的研究?长期稳定性研究?还有其他吗?
根据《药品注册年度模板(2022年版)》,“上市后研究”包括:
“按照药品批准证明文件和药品监督管理部门要求开展的上市后研究情况”
个人理解,其实就是药品批准证明文件中载明的,上市后需要继续开展的研究。后半句“药品监督管理部门要求开展的上市后研究”是个兜底条款
年度报告中上市后风险管理计划是药物警戒管理计划么?