作者:李丹编译
来源:ACDLabs CN 公众号
前言
该文章是Pfizer分析科学家发表的一篇关于AQbD理念在HPLC方法开发中的应用文章。文章结合Inlyta(阿昔替尼)有关物质方法开发过程,详细阐明了AQbD在方法开发的全过程中的应用。对于分析科学家而言,可以对AQbD理念的理解带来一定的启发。感兴趣的读者可以阅读原文,以下是对原文大部分内容的翻译。

引言
如 ICH Q8、Q9和 Q11所述,质量源于设计 (QbD) 在药物原料药和制剂工艺的开发和制造中得到很好的确立。 从高层次来看,QbD 的目标是保证工艺过程能够始终如一地提供预期性能的优质产品。 在工艺开发过程中获得的知识有助于证明设计空间和(过程)控制的建立是合理的。而可操作空间内(监管批准的)的任何设定点都将产生可接受的产品,并且工艺条件在可操作空间内的更改是(监管)可接受的。
这些相同的原则和概念已应用于方法的开发,并被称为分析 QbD (AQbD)。类似于工艺QbD,AQbD 的目标是设计一种质量可靠的分析方法,始终如一地提供预期性能。 而在方法开发、优化和验证过程中获得的知识有助于建立方法可操作设计区域 (MODR),从而获得方法的耐用性空间。
合适的(针对其预期目的)分析方法提供关键数据,以支持对药物材料(例如原料药、中间体、原料、辅料)的理解和控制。对于原料药,杂质和含量数据对于工艺的开发、优化和后续控制至关重要。对于制剂,含量和杂质方法可以帮助理解工艺过程、剂型均匀性以及与赋形剂之间的相互影响。这些方法的结果经常用于了解进行加速降解研究(有目的的降解和加速稳定性评估程序)和正式稳定性研究的原料药和制剂的降解机制。 这些方法用于确保原料药和制剂在放行和整个保质期内的质量,是确定储存条件和有效期的基础。分析方法是提供及时、高质量数据的工具,这些数据通常包含在监管文件中。因此,药物分析化学家必须确保所开发的分析方法适合其预期目的,并在整个方法生命周期内持续提供适当的数据。
然而分析方法开发没有固定模式,从使用“最喜欢的”色谱柱、固定相或供应商到使用软件辅助进行系统的方法筛选或介于两者之间的方式均可。没有“正确的”方法; 然而,更系统的方法开发工作流程将比不太系统的方法更快地更好地了解方法的分离空间和稳健性。整个方法开发过程证明该方法适合其预期目的,通过方法验证并保证后续使用。 符合其预期目的是一个关键概念,整个方法开发过程均围绕这一目的进行,必须充分了解方法需求(例如目的、特异性、灵敏度、准确度和精密度)。
在 AQbD 框架中开发的分析方法通过一系列步骤进行(图 1)。第一步是明确分析目标概况 (ATP), 从而确定方法要求和性能标准。根据方法的需要,选择一种分析技术,使方法能够满足预期的目标。根据获得的特定项目方法开发知识和经验,执行风险评估 (RA) 及识别需要进行实验设计 (DOE)评估的风险因素。 DOE 将产生 MODR 和控制策略(方法参数设置点和明确操作空间)。 MODR 内的一个点将被指定为该方法的正常操作条件 (NOC),并且NOC 条件将被验证。最后部分涉及知识管理(从方法开发、优化、验证和使用中获得的知识),应在方法的整个生命周期中保留和转移。
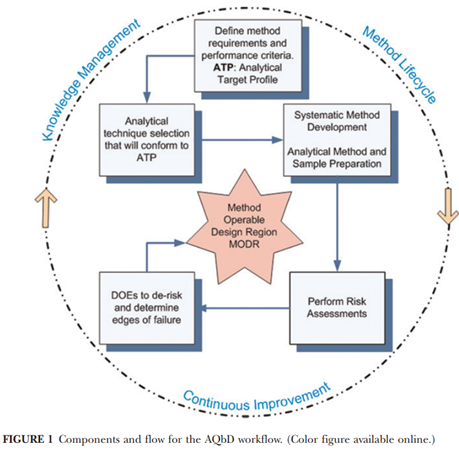
遵循 AQbD 流程开发分析方法有很多好处。 首先且最重要的是,方法将建立在对分析要求和性能的理解基础上。 由此产生的方法开发知识、方法稳健性和可转移性将使得方法更稳健,减少方法失败和转移问题。 AQbD 的另一个潜在好处包括增加监管灵活性。 这根据该方法的归档策略和监管接受程度来实现。
AQbD 概念在最近批准的药物阿昔替尼 (Inlyta) 的稳定性指示方法的开发中得到了证明。该方法开发过程充分利用了样品的结构知识和基于软件的决策支持。 AQbD 工作流程从了解方法需求 (ATP) 开始,然后是选择分析技术、制定筛选策略(Wave 1)和初步条件的优化(Wave 2 和Wave 3)、根据筛选阶段获得的知识进行风险评估,最后通过 DoE实验构建设计空间并明确可操作空间。最终获得一种稳健的色谱方法,具有易于理解的 MODR 和该方法的中心点。与传统方法相比,AQbD 工作流程的使用简化了方法开发所需的时间和资源。从接收关键预测样本集(KPSS)到确认中心点的整个 AQbD 过程大概需要两周,大约一半的时间分配给信息学方面。但是,并非所有方法都会在此时间范围内完成。
项目背景介绍
表 1 显示了本研究中每个目标化合物的结构。 这些样本构成了该方法的关键预测样本集 (KPSS)。
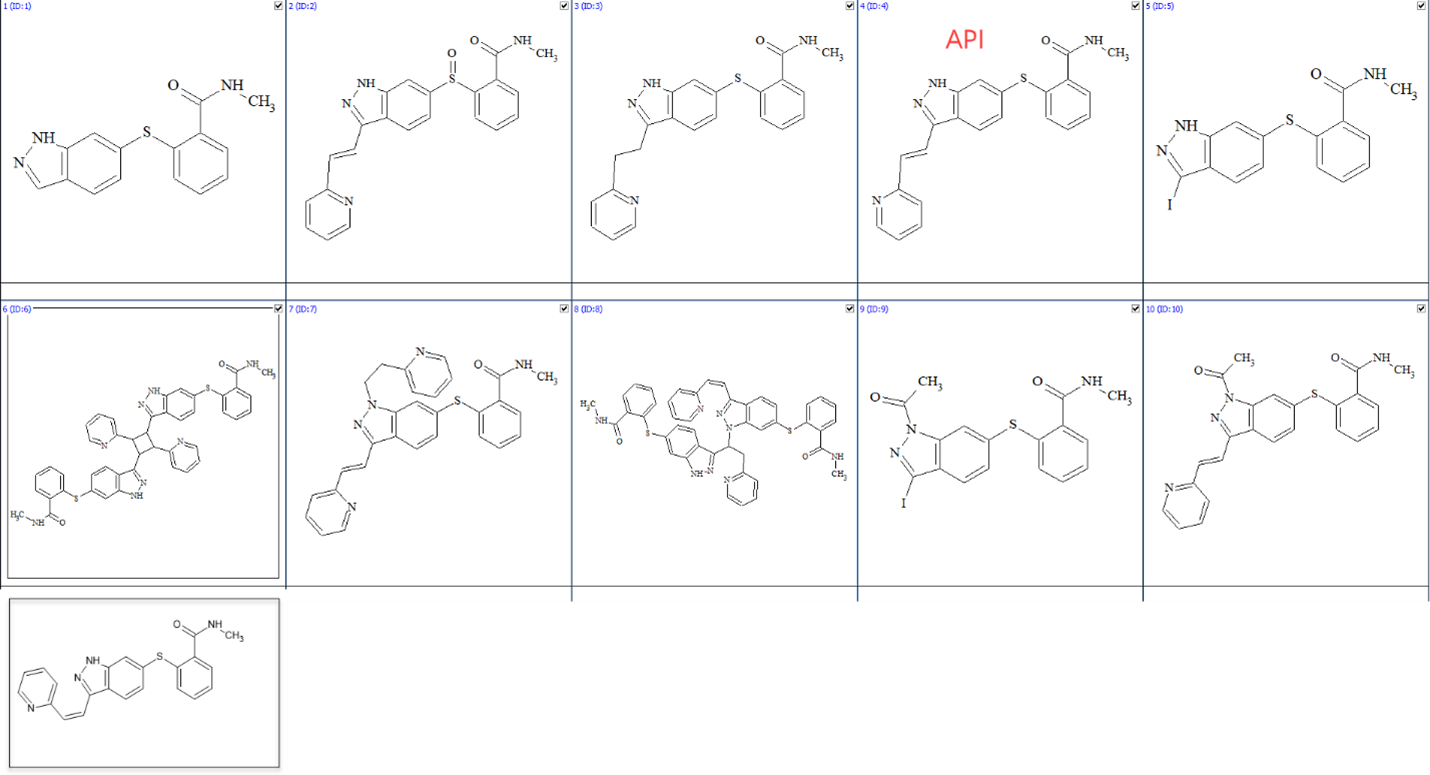
表1 目标研究对象
分析目标概况(ATP)分析
ATP 是对测量系统要求的前瞻性总结,如果达到该要求,将确保在该产品的整个生命周期内对特定产品质量属性进行准确评估。 ATP 并不限定于特定的方法或技术,因为如果任何分析技术符合 ATP 标准,则可以对其进行评估和。 下面提供了一个 ATP分析示例,用于分析阿昔替尼薄膜包衣片的含量和纯度。
含量:该方法必须能够在主浓度70-130%范围内准确定量薄膜包膜片中活性药物成分(API),并具有专属性、线性、准确性和精密度,使测量值在真实值的正负3.0%之内,且有95%的准确率。
纯度:在原料药、辅料和杂质存在的情况下,该方法必须能够在报告限和标准要求范围内准确定量与 API 相关的已知和未知杂质。方法的专属性、线性、准确度和精密度需要满足对于<0.15%水平的杂质其测量值在真实值的正负20%之内,准确率为80%;对于>0.15%水平的杂质其测量值在真实值的正负15%之内,准确率为90%。
反相色谱方法开发
许多因素都会影响色谱专属性。 通常探索的因素包括色谱柱种类、水相(pH 值和缓冲液类型)、有机溶剂类型、温度、梯度斜率等。为了获得有效的方法开发工作流程,我们制定了一个四步策略(图 2) 在进行DoE实验以获得MODR 之前,广泛探索 KPSS 的分离空间。 在此 AQbD 工作流程中,起点是获得 Log D 图(如果 KPSS 中化合物的结构已知)。 实验步骤包括评估: (1) 流动相 pH、强洗脱剂和色谱柱种类; (2) 小范围 pH 值筛选; (3)温度梯度优化。
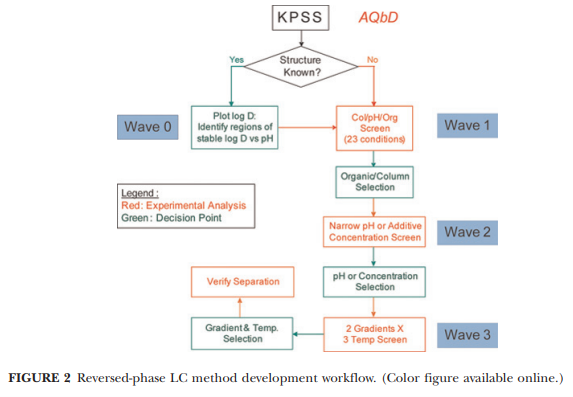
Wave 0 方法开发前的知识准备
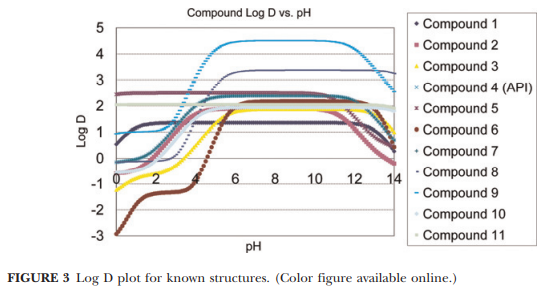
预测已知结构的目标物的 Log D值。就反相 LC 研究而言,Log D 的大小和物质保留密切相关。 所有目标分析物的pH VS Log D 的叠加图可用于直观地了解到所有目标分析物在pH 1-14范围内logD值随pH变化的情况。图 3 是本研究中使用的化合物(列于表 1)的 pH vs log D 叠加图。从该图中可以看出,在pH 6- 11 范围内,目标分析物的logD值基本保持一致,说明在该pH范围内物质的保留不受pH的调动。在pH1-6和pH>12 范围,属于log D的变动区,流动相pH的稍微变动会导致物质保留时间较大的改变,并且化合物 6 在低 pH 条件下可能无法保留。分析 KPSS 的pH vs Log D 叠加图,可以在筛选策略制定之前分析要筛选的pH条件。如果流动相 pH值选在 log D 变动区(流动相 pH 接近化合物的 pKa), 在进行色谱峰识别时需要格外注意。
Wave 1 方法筛选策略的制定
在制定方法策略时,首先对分离影响最大的色谱参数,如色谱柱种类,流动相pH和强洗脱种类进行了广泛的研究,获取对分离影响最大的关键因素信息,以便在方法优化阶段进行DoE设计时参数的选择。最终的制定的筛选策略如下表。
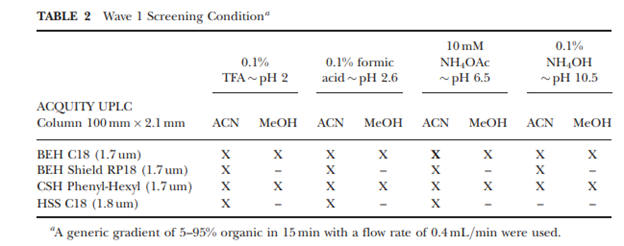
查看所有实验数据后,最后选择ACQUITY UPLC BEH C18 柱、10 mM 醋酸铵缓冲液(Ph=6.65)和乙腈溶剂作为方法优化的起点。该方法对应的色谱图如图4所示,大约 8 分钟内实现了 11 个组分的基线分离。其中选定的pH条件属于所有目标物的logD稳定区。
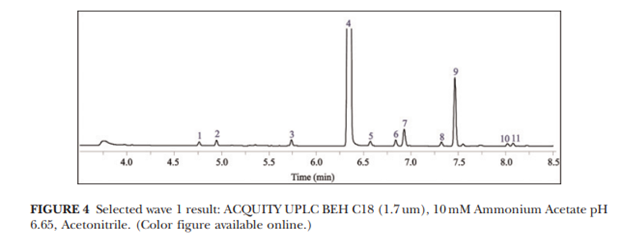
Wave 2 方法pH建模
尽管在wave1中获得了对所选条件获得了一些基本了解,但仍需要进行额外的实验,以进一步改进方法并了解其可操作范围。 在进行pH优化时色谱柱种类的有机相种类保持一致。 由于流动相 pH 值的微小变化,对分离的稳定性仍然不确定。 如果样品组中的分子在所选 pH 值附近具有 pKa,则流动相 pH 值或离子强度的轻微变化可能会显着改变选择性。 需要在较窄的 pH 范围内进行实验,以明确方法的pH耐用性范围。 Wave 2实验旨在了解 pH 值对分离的影响,最终目标是将最终方法设置在pH耐用性范围的中心处。
最终pH模型如下图所示。从图中可以看出,pH在5.8-7.0的范围内均能满足最小分离度大于1.5的要求,且当pH为6.5时分离度最大。通过pH模型不仅知道了最好pH条件为6.5,而且还知道当选定流动相pH为6.5时,方法流动相的pH值有±0.5的耐用性空间。
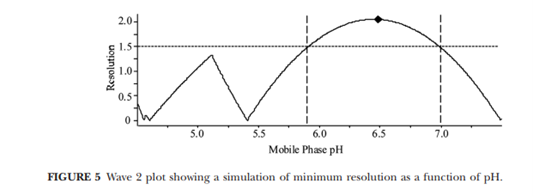
Wave 3 梯度 & 温度 2D模型
该步骤的主要目标是优化梯度和温度,以便进一步明确关键色谱峰对的分离度、运行时间和方法稳健性。通过温度和梯度两因素的DoE实验,构建出如下图所示的分离度图。图中橙色代表分离度好的区域,蓝色代表分离度差的区域。通过2D模型,可以同时研究温度和梯度两因素相互作用对关键色谱峰对的分离度影响。最后,综合考虑运行时间和分离度,选择图中红色点对应的温度和梯度条件作为最终的方法参数。
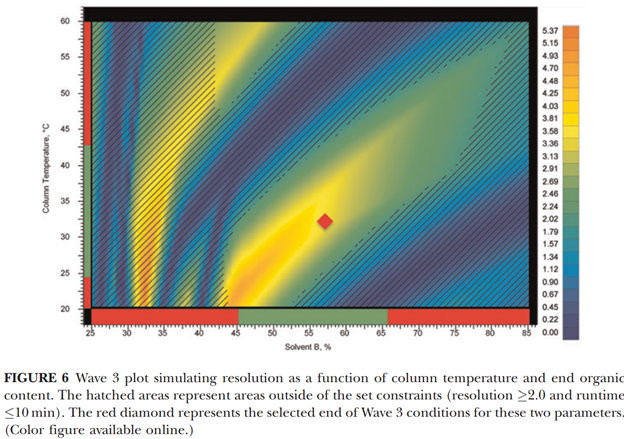
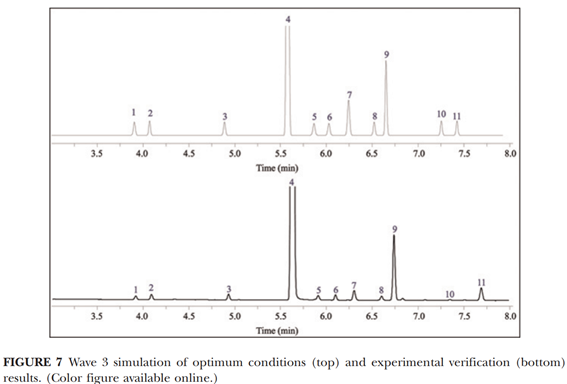
备注:FIGURE7中,上图为模型预测图谱,下图为实验获得图谱。
最后的方法参数如下表所示。
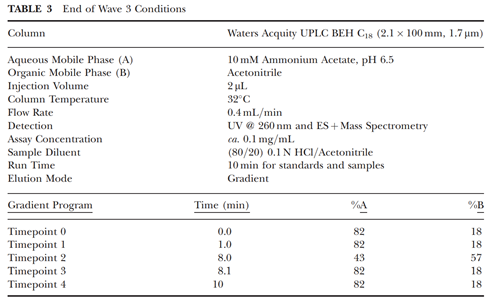
一旦确定了色谱参数的耐用性区域,将会进行风险评估(用于识别和确定风险区域的优先级)和 DoEs(确定方法条件的多元稳健性区域和潜在的失败边缘)的附加步骤。根据DoEs 评估预测替代实验条件,并通过实验确认最终方法中心点条件。最终 MODR的确定是基于从 DoEs建立的耐用性范围设置的。
风险评估(Risk Assessments,
RA)
RA是AQbD 方法开发过程中的关键步骤。如ICH Q9所述:“风险评估包括危害的识别以及与暴露于这些危害相关的风险的分析和评估。”LC 方法风险评估的目的是建立高可信度的分析方法,使其在整个生命周期中将满足所有使用条件下的所有性能标准。采用系统方法识别可能需要控制以确保方法性能的所有潜在方法因素。风险评估工具和DOEs 用于了解和管理风险领域。为了在不同的开发阶段有效地评估和降低方法风险,使用了基于分层的方法。基于 Excel 问卷的风险评估用于尚未达到 ICH 阶段的产品。问卷式 RA 方式以科学知识、RPLC 方法中常见问题为基础,侧重于“典型”方法问题评估。评估内容包括分析物物理化学特性、流动相、仪器、色谱柱和检测部分。表 4 显示了对最终Wave 3方法执行的基于 Excel的RA的分析。
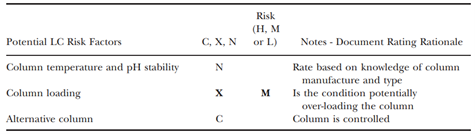
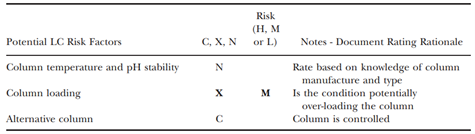
表4中各单词简称说明。(C) Control:方法中固定的实验因素; (X) Experimental:为实验研究选择的参数,以了解潜在的风险和控制水平; (N) Noise:无法控制的误差来源(例如操作员、环境因素)。
风险评分关键:(L)低风险:这个因素成为问题的可能性非常低。 风险很容易降低; (M) 中等风险:可能会影响方法属性,可以使用标准方法(例如条件、仪器、方法中指定的参数)管理风险; (H) 高风险: 风险因素可能会影响方法,并且需要通过实验研究来了解潜在的风险和控制水平。 同时为(X)和 (H)的 风险因素被视为关键参数,应通过实验 (DOE) 降低风险。
DoEs设计
从表4中可以看出,需要进行DoEs研究的实验参数有流动相pH, 柱温和梯度参数。在进行具体实验设计时,采用选中中心点后,进行高低两水平部分因子实验设计来确定方法稳健性并建立初始 MODR。该策略采用以下工作流程:
1. 中心点选取:根据wave 3中确定的条件(表 3)建立初始中心点条件。
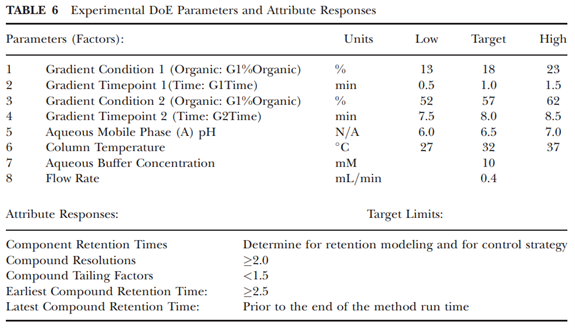
2. 因子和响应选择:选择从 RA 确定的过程参数(因子)和属性(响应),根据属性的可接受限度设置试验的低和高两因子水平。Table 6中列出了 参数(因素)和属性(响应)以及所研究的实验范围。 缓冲液浓度和流速设置为固定值,因此未在设计中进行实验评估。
3. DoE 设计选择和设计布局:这部分工作可以借助专业的统计软件完成,如Design-Expert, JMP和MiniTab等纯统计学软件。Resolution VI设计是允许确定重要主效应和双因素交互作用的统计设计。Table 7 中是采用Resolution VI设计实验运行序列,其中实验运行的随机化通过按温度水平对运行进行分组来限制,以便更轻松地执行实验。因此,中心运行在整个实验运行序列中均匀分布,以提供一种方法来测试可能在实验期间发生的系统时间效应。这种设计能够确定所有主效应和两个因素的交互作用。该设计总共包含 36 针实验,其中包括 4 个中心点,用于分析漂移、曲率和纯误差。
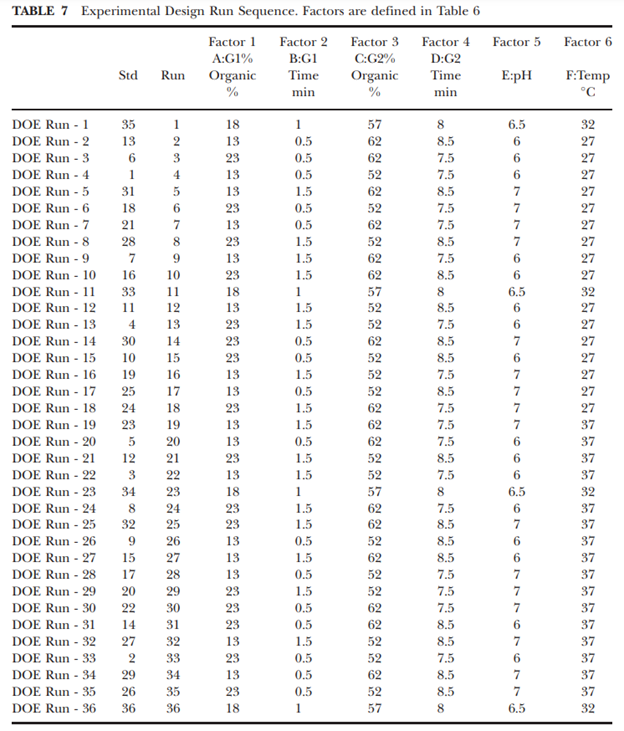
4. DOE HPLC 分析:将 DOE 设计点转换为用于 HPLC 分析的样本集。 Empower 中生成了仪器方法,以支持每个设计点的因子变化。 在每个设计点下评估样品,收集响应结果(例如化合物保留时间、分离度、拖尾)并汇总以进行统计分析。
5. DOE 统计响应分析:使用统计分析软件来评估来自 DOE 的数据。 检查所有回归模型是否存在高度共线性,定义为具有方差膨胀因子 (VIF) ≥10 的参数并确保其满足正态分布。 保留时间响应的每个回归模型的调整 r2 平≥0.999,关键分离度和拖尾响应值大于 0.99。 所有响应模型 p 值 (Prob > F) 均 <0.0001,表明模型一致性极佳,并且该模型在设计空间提供的指导有效的。
6. DOE 优化:统计分析软件用于通过使用数字和图形优化工具通过设置响应接受极限目标交来评估多响应分析。(注释:具体的统计模型分析过程就不在此详述,如读者对此感兴趣可以查看原文)。最后通过对响应曲面的分心表明,方法的中心点需要进行调整以达到最佳分离度。调整后的方法见Table 8。
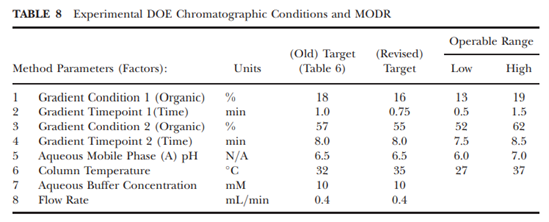
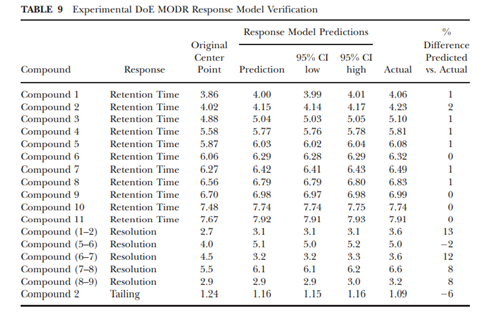
7. MODR 确定:最终的 MODR 由临界响应的实际线性方程定义,该方程设置为其各自的接受极限,对应于方法因子输入值。 因此,并非所有由表 8 中给出的可操作范围设置的因子值组合都可能产生有效的解决方案。如表 9 所示,响应模型预测与针对最终方法条件获得的实际结果非常一致,表明该模型确定的MODR具有指导意义。
结论
本文基于 QbD 原理的详细阐述了反相 LC 方法开发工作流程。工作流程从了解方法需求 (ATP) 开始,然后是技术选择、初始色谱参数的选择(wave 1)和这些条件的优化(wave 2和wave 3)、风险评估及识别和 DOE 实验风险评估。该方法利用样品的结构知识、MS 峰跟踪、自动化和基于软件的决策支持。这是一种快速有效的方法,可以最大限度地减少分析科学家花费在方法开发和数据分析上的时间,同时广泛研究实验变量。最终可生成一种稳健的色谱方法,具有易于理解的 MODR。与传统方法相比,尤其是在将方法转移相关问题考虑在内时,通过 AQbD 原理开发方法所花费的资源在方法的整个生命周期中显着减少。
Comments by 阎作伟:
预计ICH Q14 Guideline 即将于2022年上半年发布。Q14要求分析方法开发过程具有更好的科学性和系统性,确保分析方法具有很好的耐用性和可转移性。因此我们翻译了2013年Pfizer的科学家的这篇文章作为AQbD流程的介绍。在国内,能做到完整AQbD流程的单位还是少数。ACD AutoChrom其设计原理与Pfizer科学家提出的流程一致。期望在不久的将来,我们能够达到国际一流的水平。
为帮助审核人员更快处理,请填写举报原因:
为帮助审核人员更快处理,请填写举报原因:
