随着我国药品研发与国际化进程加速,“一次性进口”政策成为支持药物创新和仿制药评价的重要制度保障。本文结合现行法规,梳理药品一次性进口的适用范围、申报要点及监管框架,为研发机构与企业提供参考。
一、 适用范围与适用法规
药品一次性进口,或称“临时进口”,主要包括上市前和上市后两种情形:
(一) 上市前进口:
包括重大灾情/疫情所需药品、临床特需/急需药品、捐赠药品和研究用药品等,在尚未取得《药品注册证书》的情况下,可经国家药品监督管理局(NMPA)特别批准进口。此类药品仅限在特定范围内用于特定目的。
(二) 上市后进口:
药品再注册期间,新的注册证未获批准,同时该品种的进口药品再注册申请已经由国家药品监督管理局正式受理,并已取得药品注册受理通知书时,可以申请一次性进口。
根据现行政策,符合以下条件的研究用药品可申请一次性进口:
(一) 化学药品:
1. 以中国境内药品注册为目的的研究中用于对照药品的制剂或原料药:
2. 以仿制药质量和疗效一致性评价为目的的研究中用于对照药品的化学药品制剂或原料药。
(二) 生物制品:
1. 国内已经批准注册,但药品研发机构或者生产企业无法及时从国内市场获得的原研生物制品;
2. 国外已上市、国内尚未批准注册但已获批开展临床试验的原研生物制品。
3. 排除情形:麻醉药品、精神药品及血液制品不适用本政策。
(三) 生物类似药(在我国获批进口注册或临床试验的原研药品产地不一致的同一企业的原研药品):
1. 申请人应尽可能选择已在我国获批进口注册或临床试验的原研药作为生物类似药临床试验用参照药。
2. 为保护受试者安全,对申请人拟选择与在我国获批进口注册或临床试验产地不一致的同一企业的原研药品作为参照药的,在临床试验开始前,应提供不同产地原研药之间可比的证据或按照我国药品监管部门关于生物类似药研究与评价的相关技术指导原则要求,开展不同产地原研药品的比对研究并证明二者可比后,以补充申请方式提交国家药监局药品审评中心。待国家药监局药品审评中心审评认可后,申请人方可将未获批产地的原研药用于临床试验
二、 申请流程与审批权限
(一) 化学药品及普通生物制品
1. 受理主体:省级药品监督管理部门负责申请的形式审查与审批。
2. 办理时限:形式审查5个工作日,审评决策20个工作日。
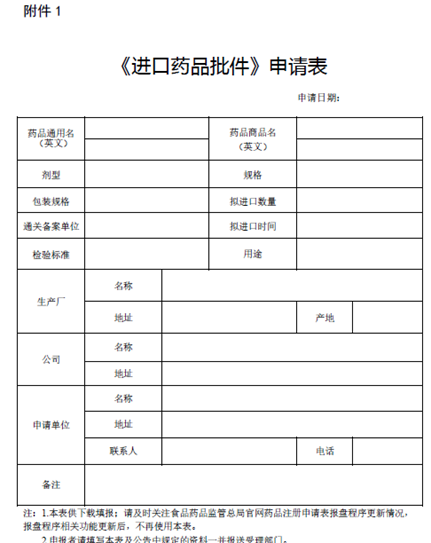
3. 资料要求:提交《进口药品批件申请表》、对照药品用途说明、质量文件等。
(二) (二) 生物制品参照药
1. 审批授权:国家药监局药品审评中心(CDE)直接受理审查。
2. 简化程序:无需重复提交已有临床试验批件的品种信息。
注:申请人负责所进口对照药品在药物研究过程中的科学性和合理性,承担所进口对照药品的质量安全、使用管理以及过程中的风险防控和处理,严格按照批准的用途使用。申请人属于委托代理的,由委托方承担上述责任与义务。
三、申报资料要求
(一) 申请人机构合法登记证明文件复印件(如营业执照、组织机构代码证等)。属于委托申请的,另须提供委托人的合法登记证明文件复印件及委托证明文件。
(二) 申请报告。内容应包括:拟申请进口对照药品的境内外上市情况、拟申请进口对照药品的来源、具体用途、数量、使用计划及拟进口药品的口岸。申请人书面承诺所进口药品不得用于上市销售及申请用途以外的其他用途。
(三) 上述申请报告及承诺须加盖申请人公章,申请人属于委托代理的,由委托方提供上述材料。
(四) 拟进口对照药品的国外获准上市证明材料(可提供上市国家药品监管部门核发的批准证明文件复印件、境外上市的药品说明书或上市国家药品监管部门网站公开信息等)。
(五) 申请人属于委托代理的,提供委托方研发机构或生产企业所在地省级食品药品监管部门出具的审查意见表。
四、进口备案要求
拟进口的对照药品应从《进口药品批件》载明的药品进口口岸进口。进口备案按照以下程序办理:
(一)申请人向口岸食品药品监督管理局提出申请办理《进口通关单》,并同时提供以下资料:
1.所进口药品的《进口药品批件》;
2.申请人机构合法登记证明文件复印件(如营业执照、组织机构代码证等)。属于委托申请的,另须提供委托人的合法登记证明文件复印件及委托证明文件;
3.原产地证明复印件;
4.货物合同复印件;
5.装箱单、提运单和货运发票复印件;
6.药品说明书及包装、标签式样(原料药和制剂中间体除外);
7.经其他国家或者地区转口的进口药品,需要同时提交从原产地到各转口地的全部购货合同、装箱单、提运单和货运发票等。
上述各类复印件应当加盖申请人公章。
(二)口岸食品药品监督管理局应按照《药品进口管理办法》的相关规定办理对照药品的进口备案。审查工作中,加强对原产地证明文件、购货合同以及发票等文件的审核,确认所进口对照药品的真实产地。
(三)口岸食品药品监督管理局审查全部资料无误后,准予进口备案,发出《进口药品通关单》。
(四)研究用对照药品的一次性进口申请,可不要求进行口岸检验。
五、 特殊情形与风险管理
1. 中药材进口:首次进口需省级药监部门审批,非首次进口直接备案(纳入目录管理)。
2. 违法后果:擅自变更用途或未备案使用者,将依据《药品管理法》追责。
参考文献
[1] NMPA-总局关于研制过程中所需研究用对照药品一次性进口有关事宜的公告(2016年第120号)
[2] NMPA-国家药监局关于临床试验用生物制品参照药品一次性进口有关事宜的公告(2018年第94号)
[3] NMPA-国家药监局关于生物类似药临床研究用原研参照药进口有关事宜的公告(2019年第44号)
[4] NMPA-进口药材管理办法(2019年)
[5] NMPA-药品进口管理办法(2003年局令第4号)
为帮助审核人员更快处理,请填写举报原因:
为帮助审核人员更快处理,请填写举报原因:

现在的省局申请一次性进口,申请表啥的每个省局的要求可能不一样,具体以的资料要求还是需要根据各省局的要求去准备。不好一概而论。